¿Cómo será la selección de los voluntarios para probar la vacuna contra el covid-19?
El inicio de las pruebas se estima para los próximos días, ya que el Instituto de Salud Pública finalizó el análisis de datos para iniciar la fase III. Serán 3.000 los participantes, quienes recibirán un suministro de "CoronaVac" en dos dosis, separadas por 15 días cada una.
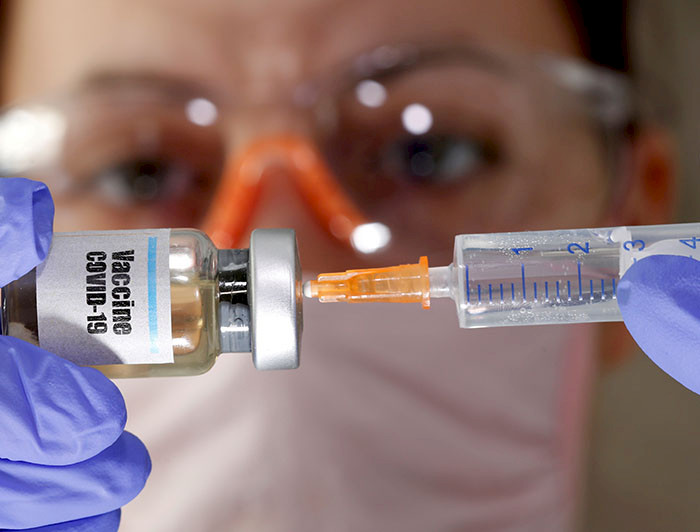
photo_camera Los académicos UC que dirigirán las pruebas sostienen que los estudios de CoronaVac han generado muy buenos resultados, tanto en materia de seguridad como de inmunogenicidad en las fases I y II. El 95% de los 50.000 voluntarios que recibieron la inoculación contra el coronavirus en China, no han manifestado efectos adversos.
Hace unos días se dio a conocer públicamente que la Comisión de Estudios Clínicos del Instituto de Salud Pública de Chile (ISP) votó favorablemente la autorización de dos estudios clínicos en fase III en Chile en vacunas para combatir el covid-19.
Una de las dos autorizadas se trata la desarrollada por Sinovac Biotech Co., Ltd., llamada "CoronaVac", que gracias al convenio de colaboración firmado por la biofarmacéutica asentada en Beijing con la Universidad Católica, el cual garantiza el acceso de los chilenos a la inmunización, ya está ad portas de comenzar la etapa en la cual se medirá la efectividad de la inmunización en voluntarios chilenos.
La vacuna de Sinovac es monovalente, lo que significa que protege contra una única cepa de un microorganismo, pero requiere dos dosis de la vacuna, los días 0 y 14, posteriormente a lo cual se efectúa también un seguimiento adecuado de su seguridad.
Esta vacuna es de virus inactivado, derivada del coronavirus cultivado en células renales de mono verde africano, posteriormente cosechado, inactivado, concentrado, purificado y adsorbido con hidróxido de aluminio.
¿Cuándo comenzará la convocatoria de voluntarios y las pruebas?
Según lo comentado por las autoridades, se anunciará en los canales oficiales institucionales durante estos días la convocatoria para enrolar a los candidatos, y así comenzar próximamente con las pruebas a fines de octubre. Si todo avanza positivamente se podría tener una vacuna el próximo año.
"Con este acuerdo nuestro país tendrá la opción de contar con al menos 20 millones de dosis en 2021, para vacunar al menos 10 millones de habitantes”- Ignacio Sánchez, rector
En efecto, como explicó el rector Ignacio Sánchez, “este protocolo incluye testear y trabajar con más de tres mil voluntarios mayores de 18 y menores de 60 años, quienes inicialmente serán reclutados desde los equipos de salud, en un proceso que dura varios meses e incluye dos vacunaciones y medición de la respuesta inmunológica. Si esta respuesta es positiva, el año 2021 podríamos tener la formulación disponible”.
Con este acuerdo nuestro país tendrá la opción de contar con al menos 20 millones de dosis en 2021, “para vacunar al menos 10 millones de habitantes”, agregó el rector.
¿Quiénes podrán participar y ser voluntarios?
Según detalló el ISP con relación a los participantes, los principales criterios que deben cumplir los candidatos que van a recibir esta prueba de inmunización, son: adultos, hombres y mujeres entre 18 y 59 años. Se exceptúa a mujeres embarazadas, personas que hayan tenido covid-19 confirmado con examen de PCR al día, y personas inmunodeprimidas. El estudio comenzará en trabajadores de la salud y luego se abrirá a otros sujetos en alto riesgo de contagio.
Además, se permite incluir personas con condiciones médicas crónicas con control adecuado y no descompensadas (diabetes, hipertensión arterial, asma), así como tabaquismo y obesidad. Como ya se ha mencionado, se espera inscribir a 3.000 participantes en el país.
Seguridad de las pruebas
El director del Instituto Milenio en Inmunología e Inmunoterapia, IMII, y académico de las facultades de Ciencias Biológicas y de Medicina UC, Alexis Kalergis, señaló que “los estudios de CoronaVac han generado muy buenos resultados, tanto en materia de seguridad como de inmunogenicidad en las fases I y II, en personas entre 18 y 59 años y en adultos sanos mayores de 60 años".
Las cifras lo demuestran. "El 95% de los 50.000 voluntarios que recibieron la inoculación contra el coronavirus en China, no han manifestado efectos adversos. Por lo tanto, las personas que participen en los análisis -a realizarse en el Centro de Estudios Clínicos de la Universidad Católica- recibirán una de las vacunas más seguras a nivel mundial”, explicó el académico.
La vacuna de Sinovac está siendo probada en Brasil, Indonesia y Turquía, países que tienen una alta circulación del virus. Aproximadamente un 5% de los voluntarios registró síntomas de baja gravedad, considerados propios de cualquier tipo de inmunización.
Kalergis enfatizó en que CoronaVac utiliza una de las técnicas más tradicionales en la producción de inoculaciones: virus inactivados. “Un método que se ha utilizado para combatir enfermedades que actualmente están controladas, como la polio”.
Este estudio de la vacuna Sinovac dura 1 año, aproximadamente, después de la primera dosis, y se realizará en los siguientes países: Brasil, Chile, Turquía, Indonesia y Bangladesh. El tiempo de duración de la inmunización se evaluará junto con los resultados de este estudio clínico.
Además, a inicios de este mes el laboratorio anunció que comenzará a testear la inmunización en niños y adolescentes entre 3 y 17 años. Aproximadamente 550 personas sanas recibirán dos dosis de CoronaVac y un placebo en ensayos clínicos, correspondientes a las fases I y II.
Este estudio de la vacuna Sinovac dura 1 año, aproximadamente, después de la primera dosis, y se realizará en los siguientes países: Brasil, Chile, Turquía, Indonesia y Bangladesh. El tiempo de duración de la inmunización se evaluará junto con los resultados de este estudio clínico.
Vigilancia del Instituto de Salud Pública
El ISP estará vigilando la correcta implementación y realización de los estudios clínicos velando por la seguridad de los participantes, mediante la notificación de eventos adversos serios que ocurran durante su desarrollo y, eventualmente, llevará a cabo una o más inspecciones del protocolo y las Buenas Prácticas Clínicas, cuando se hayan enrolado voluntarios.
Revisa el sitio de CoronaVac Fase 3 launch y entérate de todos los requisitos para participar del estudio.